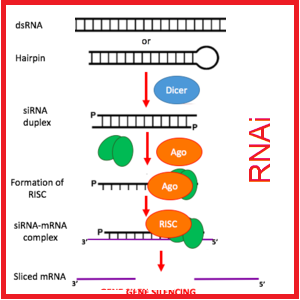
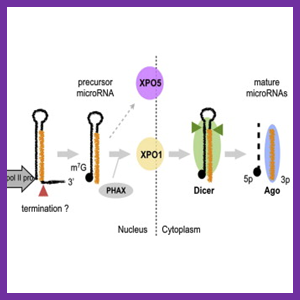
در سالهای اخیر استفاده از روش RNA مداخله گر یا RNAi به یک ابزار ارزشمند برای خاموش کردن ژنها و شناسایی عملکرد ژن ها در سطح گسترده تبدیل شده است. کاربرد RNAi تنها معطوف به کشف عملکرد ژنها با خاموش نمودن آنها در سطح پس از رونویسی نمی شود بلکه بعنوان روشی نوین جهت خاموشی فعالیت های ژنتیکی ناخواسته در درمان بیماری های مختلف نیز عمل نیز می نماید. در ادامه محدودیت های RNA مداخله گر یا RNAi در خاموشی ژنها و شناسایی عملکرد ژن ها ارائه شده است.
1- طراحی یک توالی siRNA کارآمد
آیا توالی siRNA طراحی شده قادر است به صورت موثر بیان و فعالیت یک ژن را خاموش نماید؟ محدودیت اول در روش RNAi طراحی یک توالی siRNA موثر است. محدودیتهای فراوانی برای توالی های قابل استفاده برای هدف قرار دادن ژن وجود دارد. بسیاری از این محدودیتها بستگی به نوع پلیمراز به کار رفته برای شناسایی و تکثیر توالی siRNA دارد. با این وجود حتی دنبال کردن قوانین پیشنهاد شده برای طراحی siRNA خاموشی موقت ژن هدف را تضمین نمی کند.
استفاده RNAi برای مقاصد درمانی به فاکتورهای دیگری هم بستگی دارد.اگرچه siRNA ها در شرایط کشت سلولی نسبتا پایدار هستند اما نیاز به پایداری نوکلئازی و ترمودینامیک بیشتری برای جریان در in vivo دارند. تغییرات شیمیایی siRNA برای افزایش پایداری بررسی شده است. انتخابهای مختلفی برای انواع تغییرات که باعث افزایش پایداری بدون کاهش اثر خاموشی می شوند وجود دارد و پیشرفتهایی در جهت ساخت RNA های مناسب برای درمان دیده می شود.
2- اثرات غیراختصاصی RNAi بروی سایر ژن ها و خاموش سازی ژن های غیر هدف
دو نکته بسیار مهم برای ایجاد RNAi به عنوان درمان بالینی عبارتند از :اول یافتن روش مناسب رساندن siRNA به سلولهای هدف in vivo و دوم جلوگیری از اثرات غیراختصاصی یا خارج از هدف siRNA ها. مسئله روش انتقال مشابه تمام درمانهای مربوط به استفاده از اسید نوکلئیک است.اما تأثیرات غیراختصاصی و خارج از هدف موجب کاهش فواید siRNA در تحقیقات و مصارف بالینی می شود و باید به دقت بررسی شوند. در بررسی های اولیه که موفقیت استفاده siRNA در سلولهای پستانداران گزارش کردید فرض شده بود که siRNA ها اختصاصی هستند ولی به نقشهای متعدد dsRNA کوتاه در متابولیسم سلول دقت نشده بود. با پیشرفت RNAi به عنوان یک ابزار تحقیقاتی مشخص شد که ورود dsRNA به سلول اثرات مختلفی علاوه بر خاموشی ژن هدف می تواند داشته باشد. در بسیاری موارد این اثرات واضح نیست و تنها در صورت بررسی کلی بیان ژنها قابل مشاهده است.
دو نوع اثر غیر اختصاصی کلی دیده شده است. ابتدا siRNA می تواند مسیرهای جایگزین سلولی که منجر به افزایش بیان تعداد زیادی ژن مربوط به مسیرهای ایمنی داخلی را از جمله ژنهای تحریک شونده توسط اینترفرون ( ISGs) را فعال کند.
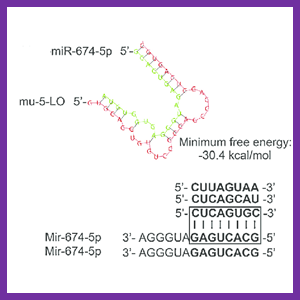
نوع دوم تأثیر که خارج از هدف نامیده شود زمانی مشاهده می شود که ژن خاصی غیر از ژن مورد نظر در واکنش به یک siRNA دچار تغییر بیان می شود. چنین اثرات خارج از هدف وابسته به توالی احتمالا مربوط به همولوژی ضعیف لازم برای فعالیت RNAi در شرایط خاصی است مثلا miRNA triggers و در نهایت از آنجا که کاربرد تحقیقاتی RNAi از مکانیزمهای سلولی مشابهی که برای تنظیم داخلی ژنها توسط miRNA به کار می روند استفاده مینماید این امکان هست که این دو فرایند با هم تداخل کنند.
3- تحریک اینترفرونی توسط siRNA
اینترفرونها (IFNs) سیتوکینهایی اند که به عنوان اولین خط دفاع ضد عفونت ویروسی در پستانداران عمل می کنند. آنها می توانند در جواب به الگوهای مولکولی خاص مختص به پاتوژنها مثل باکتری، ویروس و قارچ فعال شوند و ترشح آنها باعث حفاظت پاراکراین عفونت ویروسی می شود و همچنین واسطه واکنشهای ایمنی هستند. فعالیت این واکنش ایمنی به طور موثری توسط dsRNA تحریک می شود که یک الگوی مولکولی وابسته به پاتوژن (PAMP) شایع هنگام تکثیر ویروس است.
dsRNA مسئول شروع سه نوع رویداد پیام دهی مربوط به واکنشهای ضدویروسی است ابتدا dsRNA به پروتئینهای شناسایی dsRNA متصل می شود.نقش این پروتئینها می تواند واسطه مستقیم در فعالیتهای ضدویروسی یا شروع آبشار پیام دهی که منجر به افزایش بیان IFN و پروتئینهای ضدویروس دیگر می شود باشد.همچنین dsRNA می تواند از طریق مسیرهای غیروابسته به IFN مستقیما باعث رونویسی ژنهای خاصی شود.
در انتها باید این نکته را متذکر شد که موفقیت خاموشی ژن توسط siRNA به عوامل متعددی بستگی دارد مثل توالی siRNA انتخاب شده و ساختار آن و مساعد بودن نوع سلول برای جذب siRNA همچنین نیمه عمر mRNA و پروتئین هدف باید در نظر گرفته شوند تا خاموشی ایده ال بدست آید.